近日,山东大学第二医院朱建研究员等在Nature Communications杂志发表研究“YAP inhibits ERα and ER+ breast cancer growth by disrupting a TEAD-ERα signaling axis”。该研究揭示了雌激素受体阳性的乳腺癌中YAP蛋白扮演抑癌基因的作用。YAP蛋白可以成为潜在的新靶点逆转乳腺癌内分泌治疗耐药。

该研究启动于朱建研究员博士后阶段,历时7年。本研究由山东大学第二医院朱建教授团队、美国德州大学西南医学中心蒋进教授团队协同完成。山东大学第二医院朱建教授与美国德州大学西南医学中心蒋进教授为该研究的通讯作者。
乳腺癌是女性发病率第一位的恶性肿瘤。其中,雌激素受体阳性乳腺癌(ER positive)占乳腺癌70%的比例,因而是乳腺肿瘤最重要的亚型。雌激素受体(ER)通过启动下游信号通路的转录,对于乳腺癌的发生发展发挥至关重要的作用。尽管针对雌激素受体的调节剂他莫西芬对于乳腺癌的治疗有显著的疗效,但是内分泌治疗的耐药是乳腺癌内分泌治疗一个亟待解决的问题。因此尝试开发新的针对雌激素信号通路的靶点并揭示新的调节机制对于乳腺癌的治疗有重要的临床和科研意义。
Hippo通路最初在果蝇中证实其对于组织生长和器官发育发挥关键作用。经典的Hippo通路中,MST1/2和LATS1/2通过激酶级联反应磷酸化调控YAP从而抑制YAP入核发挥转录激活的作用。但是在MST-LATS轴不活化的时候,YAP可以进入细胞核与TEAD发生相互作用促进组织的再生。绝大部分的恶性肿瘤中显示Hippo通路因子YAP存在基因扩增和过表达促进肿瘤的进展。而在雌激素阳性乳腺癌中,该研究发现YAP蛋白比正常乳腺组织低表达;YAP的表达水平倾向于预后较好。因此,Hippo通路在雌激素受体阳性乳腺癌中的调控机制有待深入研究。
在TCGA数据库分析中,YAP的表达在ER阳性乳腺癌与好的预后相关;而三阴性乳腺癌中与差的预后相关。YAP的基因扩增多发于三阴性乳腺癌中,而YAP低表达多发于ER阳性乳腺癌中。转录组学分析显示ER阳性乳腺癌Hippo通路基因谱倾向于低表达。通过免疫组化显示YAP的蛋白水平与ER/PR呈现反相关关系。我们使用MST抑制剂激活YAP蛋白功能显示可以在体内和体外抑制ER阳性乳腺癌的生长。而过表达突变5个磷酸化位点的YAP蛋白可以获得类似的效果。MST抑制剂处理后的RNA sequence分析显示YAP蛋白可以在全基因组水平上抑制ER信号通路的靶基因水平。
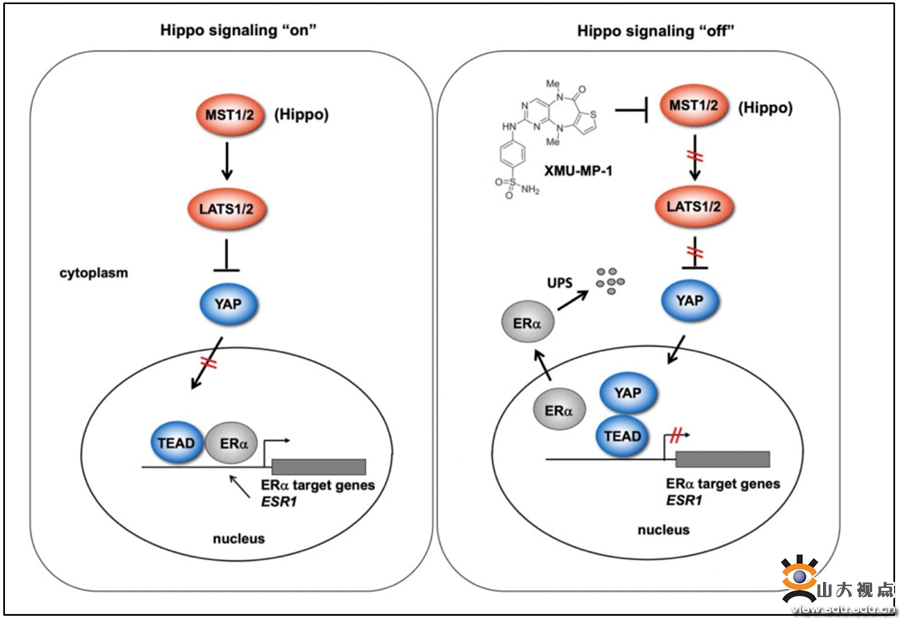
在进一步的分子机制的探讨中发现,TEAD4扮演雌激素信号通路的协同激活因子。Chip-sequence的分析中显示TEAD4和ER在基因组上有大量的系统结合的位点。而YAP的过度激活可以竞争性阻断TEAD-ER的协同作用,将ER排挤出细胞核并促进ER蛋白的降解。在PDX模型以及ER突变的乳腺癌内分泌耐药模型中,激活YAP依然可以在体内模型中阻断肿瘤的生长和进展。揭示了Hippo通路在不同肿瘤中扮演多面手的角色并为乳腺癌内分泌治疗耐药提供了新的治疗策略和思路。
朱建,山东大学第二医院胃肠外科研究员,山东省泰山学者青年专家,山东大学临床副教授,硕士研究生导师。担任山东省医学会普外科学分会委员、山东省老年医学会胃肠外科分会委员、济南市医学会结直肠肛门委员会委员。致力于消化道的恶性肿瘤的临床诊疗以及肿瘤的基础研究工作。担任Science Advance,Cancer Letter,Cell Death & Disease审稿人。发表论文14篇,其中一区文章7篇,代表性成果发表在Nature Communications,Developmental Cell,Oncogene等杂志上。承担国家自然科学基金联合基金项目,山东省自然科学基金面上项目,山东省泰山学者资助计划等课题累计到账经费190万元。研究方向:消化道肿瘤的分子机制研究、靶向药物研究、内分泌激素治疗,肿瘤高通量小分子抑制剂的筛选研究。
原文链接: https://www.nature.com/articles/s41467-022-30831-5