近日,山东大学药学院姜新义教授团队在美国国家科学院院刊(PNAS)上在线发表题为Synthetic SIGLEC9-based chimeric switch receptor augments the efficacy of CAR macrophages against glioblastoma的研究论文。该研究开发了一种基于巨噬细胞免疫检查点SIGLEC9的嵌合受体(CSR),可诱导巨噬细胞产生强烈的促炎反应和吞噬活性,显著增强巨噬细胞的杀伤能力。山东大学药学院姜新义和陈晨等为论文共同通讯作者,药学院博士研究生付志鹏、赵晓天为该论文的共同第一作者。
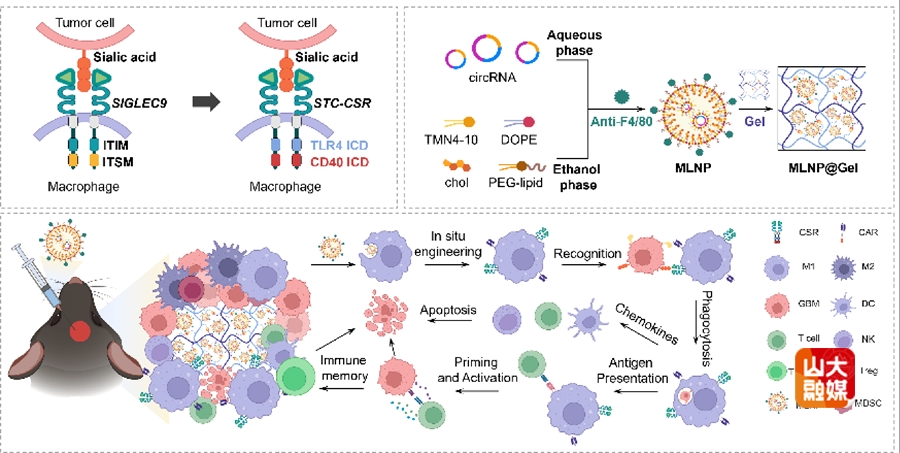
嵌合抗原受体巨噬细胞(CAR-M)疗法作为胶质母细胞瘤(GBM)的新兴免疫疗法,已展现出抗肿瘤潜能。然而,GBM表面的唾液酸聚糖通过结合巨噬细胞抑制性受体SIGLEC9,导致CAR-M发生功能衰竭,限制了其持久的抗肿瘤能力。针对这一重大挑战,研究团队开发了一种基于SIGLEC9的嵌合受体,可诱导巨噬细胞产生强烈的促炎反应和吞噬活性。实验证实,SIGLEC9的嵌合受体修饰后的CAR-M不仅能高效靶向清除肿瘤细胞,还能持续维持抗肿瘤表型。
为实现高效的体内原位重编程,研究团队开发了基于新型可电离脂质的巨噬细胞靶向脂质纳米颗粒(MLNP),实现了对肿瘤相关巨噬细胞的靶向重编程。此外,针对GBM手术易复发的临床难点,进一步构建了可注射的仿生水凝胶系统。在小鼠原位GBM模型及术后复发模型中,该体系可有效抑制肿瘤生长并防止术后复发。机制研究表明,SIGLEC9的嵌合受体功能化的CAR-M通过增强抗原呈递,促进了CD8⁺ T细胞的浸润与活化,并增加了脾脏中记忆T细胞的比例,形成了先天免疫与适应性免疫协同放大的抗肿瘤免疫效应。
本研究通过构建SIGLEC9的嵌合受体,并利用纳米颗粒-水凝胶复合系统实现了巨噬细胞的原位重编程,为攻克恶性胶质瘤提供了创新的免疫治疗策略。该研究工作得到了国家重点研发计划和国家自然科学基金等项目的资助。