近日,山东大学基础医学院医学免疫学系张利宁教授团队免疫负调控分子TIPE2与自噬调控机制的最新研究成果“TNFAIP8L2/TIPE2 impairs autolysosome reformation via modulating the RAC1-MTORC1 axis”(“TIPE2分子通过调控RAC1-MTORC1轴损伤自噬溶酶体再生”)发表于国际自噬领域TOP期刊Autophagy杂志(中科院JCR期刊1区,5年影响因子IF:11.8)。该论文以山东大学为第一通讯作者单位,基础医学院医学免疫学系博士生李文为第一作者,张利宁教授和李艳老师为共同通讯作者。
自噬是一种高度保守的细胞内降解途径,在细胞代谢、生存和衰老等多种生理过程中发挥重要作用,其功能异常与多种疾病的发生和发展有关。自1955年首次发现自噬囊泡以来,自噬领域已经两次获得诺贝尔生理学和医学奖,可见其重要价值。自噬调控机制的研究是自噬领域的关键问题,也是干预治疗的基础。张利宁教授团队创新性发现新的免疫负调控分子TNFAIP8L2/TIPE2 (tumor necrosis factor, alpha-induced protein 8-like 2) 不仅调控自噬小体的形成,更重要的是调控自噬诱导溶酶体的再生,进而影响自噬流。TIPE2的过表达损伤自噬流,诱导肿瘤细胞死亡,发挥抗肿瘤作用;TIPE2的敲除或沉默,改善自噬流,导致免疫细胞过度活化并引起过强的炎症反应。
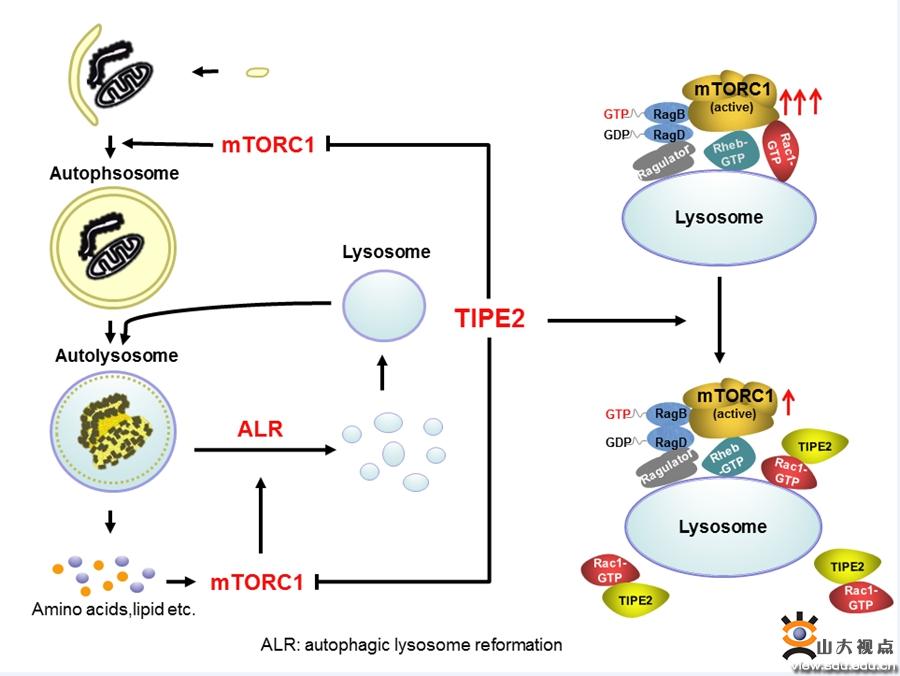
从分子机制上发现TIPE2可通过与MTOR竞争性结合GTP-RAC1,抑制MTORC1在溶酶体上活化,负调控MTORC1的活性,提出了TIPE2通过RAC1-MTORC1轴调控自噬流及细胞死亡的新机制,为以TIPE2为靶点治疗肿瘤和免疫相关疾病提供了理论依据。
TIPE2是山东大学校友、美国宾夕法尼亚大学陈有海教授团队在国际上首先发现的免疫负调控分子,陈有海教授与山大多个科研团队开展合作,张利宁教授团队和陈有海教授合作研究的相关成果先后发表在Molecular Cell和Molecular Cancer等杂志。上述研究得到国家自然基金、山东省重点研发(重大科技创新工程项目)计划等项目的资助。激光共聚焦显微镜数据工作得到基础医学院显微表征平台大力支持。
相关链接:https://doi.org/10.1080/15548627.2020.1761748